Quanti di voi sanno che cos’è il pH? Stiano zitti i chimici, i periti chimici e tutti coloro che hanno studiato, ad un qualsiasi livello, la chimica.
Bene. Mi perdoneranno tutti coloro che hanno studiato o studiano la chimica, ma devo dare la definizione di pH a tutti coloro che non hanno idea, se non vaga, di cosa significhi questa parola.
Non è una parola magica; non è neanche un rito magico di carattere esoterico. Si tratta semplicemente di un modo che i chimici usano per riportare quella che è la concentrazione di ioni idrogeno (H+) in una soluzione acquosa. Mi diranno i chimici più estremi che il pH si può valutare anche per sistemi organici. Ma io non voglio essere estremo e mi attengo alla chimica più tradizionale, per cui mi fermo al fatto che la misura del pH è quella che si fa per le soluzioni acquose.
Il pH è il logaritmo in base 10 dell’inverso della concentrazione idrogenionica:
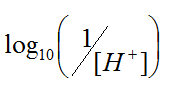
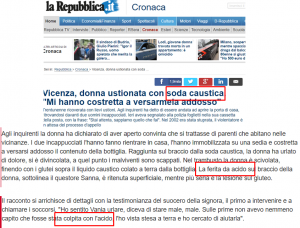
Anche la casalinga di Voghera sa che se il pH è inferiore a 7 si parla di sistemi acidi; se il pH è superiore a 7 si parla di sistemi basici; se il pH è proprio 7, allora si parla di sistemi neutri. Il problema è che, al di fuori del contesto chimico, le parole “acido”, “base” e “neutro” sono prive di significato. Ad usare in modo improprio termini che hanno un significato ben definito nel linguaggio scientifico ci si mettono anche i giornalisti. Per esempio cliccando qui si apre una pagina di Repubblica.it in cui si legge che una donna è stata aggredita ed è stata costretta a versarsi addosso della soda caustica. Per effetto di questa aggressione la donna ha subito ustioni da “acido”. Non ci credete? Allora cliccate sul link anzidetto oppure leggete la Figura 1 in cui ho evidenziato l’incongruenza tra “soda caustica”, che è una base, e “acido”, che nell’opinione comune è qualcosa che fa male.
Ma veniamo al punto principale di questa nota.
L’equilibrio di dissociazione dell’acqua si può scrivere in questo modo:
![]()
Questo equilibrio è governato da una costante alla quale è stato dato il nome di “prodotto ionico dell’acqua” che ha la forma:
![]()
Il valore del prodotto ionico dell’acqua è 1.0 x 10-14 M2 quando la temperatura è 25 °C. È facile calcolare il pH al punto di neutralità, ovvero quando la concentrazione degli ioni idrogeno è uguale a quella degli ioni ossidrile. Al punto di neutralità il valore di pH è 7.
Ciò che in genere molto spesso si dimentica è che le informazioni contenute nelle righe precedenti sono valide solo ed esclusivamente alla temperatura di 25 °C. Infatti, i valori delle costanti di equilibrio (ed il prodotto ionico è una costante di equilibrio) dipendono dalla temperatura alla quale si ha l’equilibrio chimico. La Figura 2 mostra come cambia il prodotto ionico dell’acqua al variare della temperatura.
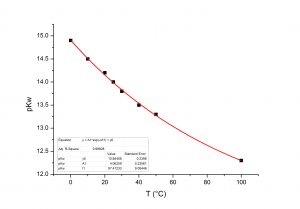
La Figura 3, invece, fa vedere il cambiamento del valore del pH in funzione della temperatura. Più è alta la temperatura più si abbassa il valore del pH relativo alla condizione di neutralità come conseguenza dell’indebolimento dei legami covalenti tra ossigeno ed idrogeno nell’acqua. A 100 °C, il valore del pH all’equilibrio è circa 6.1. Questo valore non indica acidità, bensì neutralità a quel valore della temperatura.
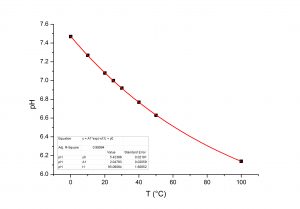
Ciò che è valido per l’equilibrio di dissociazione dell’acqua è valido per tutti i tipi di equilibrio. Per esempio, la dissociazione dell’acido acetico in acqua segue l’equilibrio:
![]()
La costante di equilibrio ha la forma:
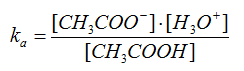
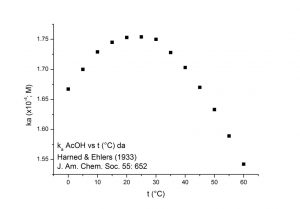
Il valore della ka a 25 °C è 1.75 x 10-4 M. Da un lavoro pioneristico del 1933, si ricava il grafico di Figura 4 che mostra la variazione del valore della costante acida dell’acido acetico al variare della temperatura nell’intervallo 0-60 °C.
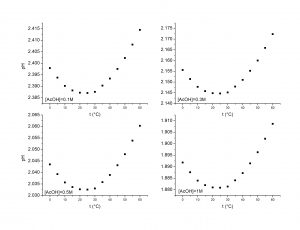
Utilizzando valori differenti per le concentrazioni pre-equilibrio di acido acetico, è facile ricavare il grafico di Figura 5 che mostra come cambia il valore del pH nelle condizioni di equilibrio al variare della temperatura.
In sintesi, il valore del pH di una qualsiasi soluzione acquosa dipende da numerosi fattori tra cui: natura e concentrazione del soluto e temperatura del sistema.
Quando si considerano sistemi complessi in cui l’equilibrio acido/base è regolato dalla presenza di più coppie acido/base differenti, oltre alla temperatura, bisogna tener conto anche degli equilibri di dissociazione multipli. Per esempio, la valutazione del pH all’equilibrio per soluzioni di acido fosforico (H3PO4) va fatta considerando le seguenti condizioni:
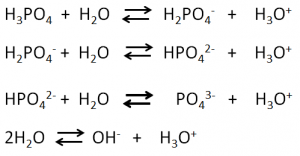
Ad ognuno degli equilibri descritti è associata una costante il cui valore cambia in funzione della temperatura. Si capisce, quindi, che la valutazione del pH all’equilibrio diventa sempre più difficile all’aumentare della complessità del sistema.
Anche la presenza di sali altera i valori delle costanti di equilibrio. Per esempio la costante acida del secondo equilibrio dell’acido fosforico risente della forza ionica come indicato in Figura 6.
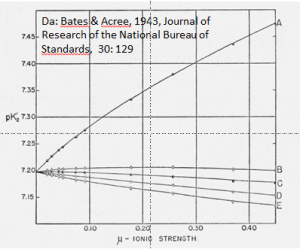
Riassumendo, il pH all’equilibrio per sistemi complessi contenenti coppie acido/base di natura differente dipende da natura del soluto, concentrazione del soluto, temperatura e forza ionica.
Fonte dell’immagine di copertina: http://alcyonitalia.com/items?key=_-57&keyType=I


